El cáncer de laringe en general, y especialmente el cáncer supraglótico, es una enfermedad locoregional porque antes o después en su evolución natural ha de comprometer a los ganglios linfáticos del cuello, con las connotaciones diagnósticas, terapéuticas y de pronóstico que ello comportará.
Atendiendo a la clasificación topográfica, la más utilizada en la clínica, el cáncer supraglótico es aquél de extensión comprendida y limitada entre el borde libre de la epiglotis y un plano horizontal que pasa por encima de las caras superiores de las cuerdas vocales verdaderas. No obstante, en hasta un 34,1% de los casos no es posible estimar el origen real del cáncer debido al estadio avanzado del tumor: tumores gloto-supraglóticos o transglóticos. (Maier y Tisch, 1997).
Desde el punto de vista histopatológico, la mayoría de ellos son carcinomas epidermoides o escamosos (99%). El rico drenaje linfático del territorio supraglótico favorece una temprana diseminación cervical bilateral del proceso neoplásico, incluso en estadios iniciales y con pequeños volúmenes del tumor primario. Efectivamente, el riesgo de enfermedad ganglionar oscila entre el 25 al 80%. Los niveles más frecuentemente afectados son los ganglios subdigástricos y yugulares medios y altos (áreas II y III) y los retrofaríngeos. Las metástasis a distancia en el cáncer de laringe son relativamente infrecuentes, se relacionan con los estadios T y N avanzados, y se localizan fundamentalmente en pulmón, hueso, hígado y cerebro. (Por ello existe la recomendación de solicitar estudio por PET-TC en tumores T≥3)
Esencialmente desconocida, podemos hablar en general de factores etiológicos exógenos y endógenos con los que se ha asociado el cáncer de laringe.
Los factores exógenos son con diferencia los más influyentes: alcohol (cocarcinógeno en la glotis y la subglotis, carcinógeno en la supraglotis) y tabaco (carcinógeno en toda la laringe), de actividad carcinogénica multiplicativa y dosis-dependiente (Cattaruzza et al, 1996): efectivamente, en el vestíbulo laríngeo el alcohol realiza su acción oncogénica por contacto directo con la epiglotis y los repliegues aritenoepiglóticos y la inflamación difusa etílica de la VADS favorece la acción carcinogénica de los hidrocarburos del tabaco.
Otros factores exógenos más controvertidos pero a tener en cuenta son: dieta pobre en verduras, lácteos y frutas, medioambientales y de exposición laboral (hidrocarburos aromáticos y policíclicos, polvos metálicos, cementos y lacas, asbesto, amianto, polvo de madera y piedra), las radiaciones ionizantes (factor infrecuente y controvertido) y el virus del papiloma humano y del herpes simple (Álvarez et al, 1996). Efectivamente, desde el año 2015 el cáncer de laringe se considera una enfermedad profesional en los trabajadores expuestos al amianto (asbesto).
De los factores endógenos, el más característico es el grupo de las laringitis crónicas hipertróficas con displasia, dónde es el grado de displasia el responsable del potencial de malignización (y favorecido por el abuso continúo del tabaco). El reflujo laringofaríngeo (controvertido, con una Odds Ratio de hasta 2,11 (Vaezi et al, 2006), demostrado en un 26,4-53,5% de los pacientes operados de laringectomía total o parcial en los primeros dos días del postoperatorio (Marín Garrido et al, 2007)) y el abuso fonatorio son otros factores que podrían tener su papel de forma no aislada en el cáncer de laringe. También ha de considerarse la genética, tanto por el comportamiento epidemiológico (antecedentes familiares demostrados en hasta el 20% de los casos) como por el etiopatogénico: sobreexpresión de oncogenes y pérdida de función de genes supresores en el origen del cáncer (ej.: mutación gen p53); en definitiva heredamos la capacidad de reparación del ADN. El factor hormonal: la predominancia del cáncer de laringe en el sexo masculino (razón de hasta 10:1) postula la presencia de receptores androgénicos en el cáncer de laringe, ausentes en un epitelio normalizado. Y finalmente hemos de considerar el factor favorecedor del desarrollo de un cáncer de laringe (o de cualquiera) de la inmunodeficiencia: las células cancerígenas son antigénicas, y “deberían ser reconocidas y eliminadas por un sistema inmune competente”.
En general el cáncer de laringe es el más frecuente de los tumores malignos de cabeza y cuello, el segundo más frecuente en la vía respiratoria alta por detrás del de pulmón. Y aun así sólo representa el 1-2% de todos los tumores malignos del organismo.
En España alcanza una incidencia del 2,2 al 4,8% (de las más altas del mundo, especialmente en el sexo masculino), y es el responsable del 1,5 al 2,5% de las muertes producidas por tumores malignos.
Tiene una marcada predisposición por el sexo masculino (6-7:1) aunque tiende a equipararse en el norte de Europa y en relación al aumento en el consumo del tabaco y del alcohol, en la mujer. Tiene un pico de edad de máxima incidencia entre los 55 y 65 años (de 60-70 años en el sexo masculino).
A partir de los años 80 se produjo un cambio en la localización más frecuente del cáncer de laringe en los países latinoamericanos y mediterráneos como España: la localización supraglótica dejó de ser la más frecuente a favor de la glótica (60-65% vs 30-35%). Fue al menos hasta 2003 la neoplasia con más alta razón hombre:mujer en la mayoría de las poblaciones. El cáncer supraglótico representa de un 15-60% del cáncer de laringe.
ANATOMÍA PATOLÓGICA:
La mayoría de los tumores malignos de la laringe derivan de la transformación maligna de una metaplasia escamosa del epitelio de revestimiento malpighiano, es decir, son carcinomas epidermoides. De hecho el 95-98% serán carcinomas espinocelulares, por estar formados por células similares a las del estrato espinoso, con grados histopatológicos de diferenciación variables, de bien a moderado o indiferenciado.
Existen algunas variantes de carcinomas epidermoides, y en la laringe las más frecuentes son:
- El carcinoma verrucoso, exofítico y de aspecto macroscópico similar al papiloma córneo, con características citológicas de benignidad aunque con invasión en profundidad y abundante infiltrado inflamatorio;
- El carcinoma sarcomatoide, de células fusiformes o seudosarcomatoso, con celularidad maligna tanto epitelial como conjuntiva, con estudio inmunohistoquímico epitelial, de aspecto macroscópico vegetante, polipoide y friable.
Otra estirpe celular susceptible de degeneración maligna y especialmente abundante en la supraglotis es el epitelio glandular seromucoso exocrino: adenocarcinoma, carcinoma adenoide quístico y carcinoma mucoepidermoide.
Mencionar también a las neoplasias malignas derivadas del tejido conjuntivo de la laringe: condrosarcoma, fibrosarcoma, rabdomiosarcoma y leiomiosarcoma entre otros; y a las metástasis laríngeas de otros tumores malignos, fundamentalmente el adenocarcinoma de riñón y el melanoma de piel.
En las primeras fases de evolución del cáncer laríngeo la sintomatología depende de la localización del tumor.
En el caso concreto del cáncer supraglótico también podemos distinguir entre dos regiones que se comportan clínicamente de modo diferente:
- el vestíbulo laríngeo, formado por la epiglotis alta y los repliegues ariepiglóticos, dónde domina una sintomatología deglutoria; y
- la parte inferior de la supraglotis, formada por el pie de la epiglotis, las bandas y los ventrículos de Morgagni, de sintomatología fonatoria.
El cáncer supraglótico produce una sintomatología al inicio larvada y escasa, común además a multitud de enfermedades más frecuentes y banales. Hablamos de parestesias faríngeas (IX y Xpc) referidas como sensación de cuerpo extraño en la garganta y necesidad de carraspeo; disfagia y/o odinofagia con otalgia refleja.
Es la persistencia y el agravamiento en el tiempo de esta sintomatología, además de los factores de riesgo del paciente, lo que nos sugerirá el diagnóstico. Todo esto contribuye a un diagnóstico más tardío y en unos estadios más avanzados. Los tumores glóticos se diagnostican en estadios más precoces que los supraglóticos (83,1% vs 60,9% en T1-2; 73,46% vs 10,83% en T1; Tamarit Conejeros et al, 2007). Deben influir razones como la precocidad de aparición del síntoma disfonía en el cáncer glótico y la concienciación de la población Española para acudir a su especialista cuando ésta se presenta.
Con el tiempo el cáncer se hace transglótico y entonces también se suma la clínica respiratoria: disfonía (la voz del cáncer supraglótico suele ser más gangosa o en patata caliente) y disnea (típico de tumores supraglóticos ya avanzados).
Recordar que hasta un 10-40% de los casos se presentan por vez primera con una adenopatía cervical lateral palpable.
Como bien se ha comentado, en estos tipos de tumores, en cuyos inicios existe una escasa sintomatología, debemos de tener un especial cuidado de aquellos pacientes con antecedentes personales importantes, de alcohol, tabaco, etc...
La inspección y la palpación cervical permiten identificar y caracterizar las adenopatías metastásicas tan frecuentes en el cáncer supraglótico. Son duras e indoloras, y estarán fijadas a los planos profundos o superficial (piel) cuando existe rotura capsular.
Los tumores supraglóticos son muy linfófilos, presentándose con adenopatías clínicamente positivas en hasta el 40-55% de los casos (75% en el diagnóstico), y frecuentemente bilaterales (1/3 en el diagnóstico; 40-50% antes de dos años).
Una excepción, los tumores de ventrículo de Morgagni que suelen producir adenopatías unilaterales. (Lahoz Zamarro et al, 2001). Lamentablemente es frecuente la existencia de metástasis cervicales ocultas tanto a la exploración clínica como a las pruebas de imagen convencionales.
La palpación cervical, obligatoria, tiene un índice elevado de falsos negativos en la detección de adenopatías en los espacios cervicales profundos (mediales al paquete vascular yúgulo-carotídeo), o cuando éstas son de pequeño tamaño, o en cuellos gruesos, o en pacientes sometidos a tratamientos radioquimioterápicos. La ausencia de crepitación laríngea o signo de Mouré hará sospechar la exteriorización posterior del cáncer laríngeo.
Consideramos que el uso generalizado, y discutible, de la laringoscopia indirecta, que realizamos aún en todos nuestros pacientes que vienen a la Unidad de Cabeza y Cuello, podría tener mucha relevancia en una primera evaluación de este tipo de tumores, pues nos expone de forma fácil, rápida y tolerable, una primera visión de este área supraglótica. Con ella se consigue una primera imagen de posición, invasión de base de lengua, afectación de la región aritenoidea, que nos ayudará sin duda a decidir el orden y necesidad de las distintas pruebas de imagen.
Endoscopia flexible y rígida. El uso necesario de ambos lo realizamos siempre en la primera consulta de nuestros pacientes. En el caso de presencia de un tumor con exteriorización desde la supraglotis, hacia vallecula, repliegues y base de lengua, adquiere mayor necesidad el uso del endoscopio rígido, recomendando el de 70º para este área.
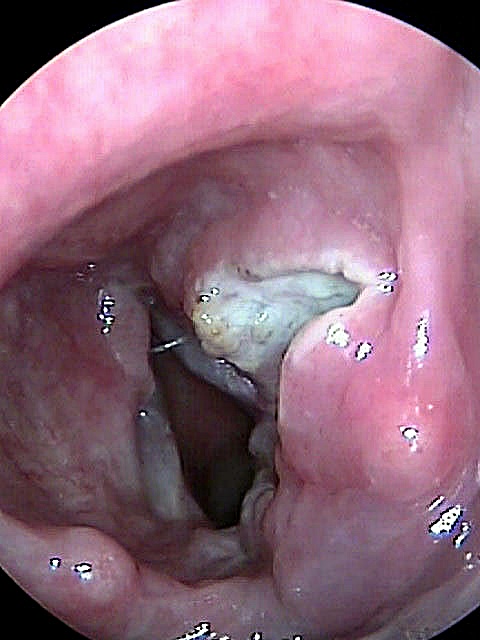
Tumor supraglótico izquierdo, con afectación aritenoidea
Sistema NBI (Narrow Band Imaging). La incorporación de estos sistemas en nuestras torres de videoendoscopia de alta definición, nos aporta una gran ayuda a estas áreas supraglóticas e hipofaríngeas, por la posibilidad de acercarnos en busca de los distintos patrones sospechosos descritos en la literatura (ver lecturas recomendadas).
El sistema NBI (imagen de banda estrecha) consiste en utilización de un sistema de filtros que estrecha la longitud de onda de la luz emitida. Los sistemas NBI actuales se basan en dos bandas, correspondientes a la luz azul y verde.
La luz de color azul tiene una longitud de onda corta, penetra poco en la pared del órgano estudiado y refleja las imágenes más superficiales. Esta luz es absorbida por la hemoglobina, de modo que se resalta la red capilar próxima a la superficie mucosa.
La luz verde penetra más, y reproduce los vasos de mayor profundidad. Esta técnica de endoscopia sería de utilidad en la detección precoz de tumores faringolaríngeos.
También para valorar la invasión en profundidad del cáncer de faringe, o incluso para el seguimiento de pacientes tratados con radioterapia. Si mediante las imágenes de endoscopia convencional las lesiones sospechosas se muestran por cambios en la coloración o la regularidad de la mucosa, las imágenes de banda estrecha identificarían alteraciones en la estructura microvascular.
Se muestran como áreas parduzcas, que tras la magnificación dejan ver un punteado marrón disperso. Por su epitelio fino escamoso y no queratinizado, la laringe y la hipofaringe serían lugares ideales para aplicar el sistema NBI, que permitiría apreciar cambios neoangiogénicos sutiles asociados a lesiones neoplásicas y precancerosos.
Lo hemos utilizado en quirófano, donde nos da bastante información en la cirugía parcial, para determinar los bordes tumorales y por tanto el límite de seguridad a resecar.

Lesión incipiente por NBI en supraglotis izquierda
Estroboscopia. Aunque en nuestra unidad la realizamos a todos los pacientes oncológicos, sólo tendría una utilidad en aquellos tumores bajos de la supraglotis, donde no podemos ver bien el borde inferior tumoral, aportandonos información limitada de la afectación de esa cuerda vocal con alteraciones de movilidad, onda mucosa, etc
TAC cervical con contraste. Es la prueba de imagen inicial, que pedimos urgente en la primera consulta en todos los pacientes con carcinomas laríngeos. Nos aporta muy buena información de la extensión tumoral, afectación de partes blandas y estado de ganglios cervicales. En sospecha de T3-T4, ampliaremos a TAC cérvico-torácico, siguiendo el protocolo de nuestro centro.

RNM cervical con contraste, se ha mostrado superior para la valoración del espacio preepiglótico, la base de la lengua y la infiltración cartilaginosa, y por tanto indispensable en el cáncer de supraglotis. Lo solicitamos, siempre que vemos la exteriorización tumoral hacia estas regiones.

Gammagrafía con Tl 201: Es una técnica de medicina nuclear que estudia el metabolismo celular. Podría tener interés, en aquellos problemas diagnósticos que presentan las técnicas de imagen convencionales, TC y RMN, en el diagnóstico diferencial de pacientes postratamiento (cirugía, quimioterapia o radioterapia) y/o tumor residuales, recidiva o necrosis, sobre todo en aquellos centros donde no se dispone aún del PET-TAC
PET-TAC. Tomografía por emisión de positrones. La TC y la RMN de forma aislada o complementaria no han optimizado el número de verdaderos positivos ni anulado el de falsos negativos en la enfermedad cervical metastásica y por tanto, cuando sea posible, sería ideal incluir la tomografía por emisión de positrones en los protocolos de diagnóstico del cáncer de cabeza y cuello (algo obligado en nuestro centro, al menos en los T3, T4). Las listas de espera, y el elevado coste económico, hacen que no se solicite a todos los tumores supraglóticos, pero terminará imponiéndose.
Debemos descartar la presencia de metástasis a distancia, hecho infrecuente al diagnóstico y que representa menos del 0,5-1% de los casos: examen físico general, hemograma con enzimas hepáticas y al menos una radiografía de tórax (que nosotros sustituimos por TC cérvico-torácico).
La afectación cervical metastásica confirmada por histología (Np), y su número (≥3), son el factor pronóstico más importante en la aparición de la metástasis a distancia del cáncer de laringe y en la supervivencia (León et al, 2000; Lahoz Zamarro et al, 2001). También influyen en la supervivencia y en el riesgo de recidiva locoregional la presencia de afectación capsular del ganglio (de controvertida relación con el tamaño de la adenopatía) y la afectación multinivel.

PET-TAC. Captación tumoral en vallecula izquierda
GENERALIDADES
Describiremos los estadiajes de los tumores supraglóticos, siguiendo los criterios de la AJCC Laringeal.
CLASIFICACIÓN: TNM
- T: Tamaño y localización del tumor
- T1 Tumor confinado a un subsitio de la supraglotis, con movilidad normal de las cuerdas vocales.
- T2 El tumor invade la mucosa de más de un subsitio adyacente de la supraglotis o la glotis, o una región fuera de la supraglotis (por ejemplo, la mucosa de la base de la lengua, la valécula, la pared media del seno piriforme) sin fijación de la laringe.
- T3 El tumor está confinado en la laringe, con fijación de una cuerda vocal o invade cualquiera de los siguientes sitios: área poscricoidea, espacio preepiglótico, espacio paraglótico o corteza interna del cartílago tiroides.
- T4a Enfermedad local moderadamente avanzada. El tumor se disemina a través del cartílago tiroides o invade los tejidos más allá de la laringe (por ejemplo, la tráquea, los tejidos blandos del cuello, incluso el músculo extrínseco profundo de la lengua, los músculos fusiformes, la tiroides o el esófago).
- T4b Enfermedad local muy avanzada. El tumor invade el espacio prevertebral, reviste la arteria carótida o invade las estructuras mediastínicas.
- N: Diseminación ganglionar regional
- NX No se pueden evaluar los ganglios linfáticos regionales.
- N0 No hay metástasis en los ganglios linfáticos regionales.
- N1 Metástasis en un solo ganglio linfático ipsilateral, ≤3 cm en su dimensión mayor.
- N2 Metástasis en un solo ganglio linfático ipsilateral, >3 cm, pero ≤6 cm en su dimensión mayor. Metástasis en múltiples ganglios linfáticos ipsilaterales, ninguno >6 cm en su dimensión mayor. Metástasis en ganglios linfáticos bilaterales o contralaterales, ninguno >6 cm en su dimensión mayor.
- N2a Metástasis en un solo ganglio linfático ipsilateral, >3 cm, pero ≤6 cm en su dimensión mayor.
- N2b Metástasis en múltiples ganglios linfáticos ipsilaterales, ninguno >6 cm en su dimensión mayor.
- N2c Metástasis en ganglios linfáticos bilaterales o contralaterales, ninguno >6 cm en su dimensión mayor.
- N3 Metástasis en un ganglio linfático, >6 cm en su dimensión mayor.
- M: Metástasis a distancia:
- M0: Ausencia de metástasis
- M1: Presencia de metástasis
TRATAMIENTO EN FUNCIÓN DE LOS ESTADIOS (TNM)
T1-2 N0 supraglótico.
Opciones quirúrgicas: Primera opción en nuestro protocolo. La supraglotis tiene un suministro linfático abundante y, como consecuencia, el riesgo de enfermedad ganglionar es significativamente mayor para los cánceres supraglóticos T1-T2 que para los cánceres glóticos T1-T2. Por lo tanto, en nuestro protocolo hospitalario, incluso en ausencia de evidencia clínica o radiológica de afectación ganglionar, se recomienda el tratamiento electivo de al menos los niveles ganglionares bilaterales II y III, ya sea con RT o disección selectiva del cuello. Empiezan a aparecer estudios, donde los N0 con PET-TAC negativo, no se realizaría de entrada, el tratamiento cervical, sin cambios de supervivencia a 5 años, lo que acabará condicionando nuestro manejo actual.
- Resección de la lesión por vía endoscópica con láser C02. Nuestro grupo, hemos realizado antes de disponer del láser C02, resecciones con agujas de Tungsteno con resultados similares al láser. Vaciamiento selectivo ambos lados del cuello, a veces diferido en dos o tres semanas después de la resección endoscópica. Si el estudio de las piezas quirúrgicas informa de características desfavorables*, radioquimioterapia concomitante. Si sólo hay un ganglio positivo, y no hay características desfavorables, radioterapia de forma opcional.
- Laringectomía parcial horizontal supraglótica por vía externa, con vaciamiento selectivo de ambos lados. El resultado del estudio postoperatorio de las piezas, condiciona de la misma forma que en el apartado anterior, recurrir o no a los tratamientos adyuvantes. La laringectomía supraglótica abierta puede tener un papel en casos seleccionados en unidades con experiencia quirúrgica adecuada y servicios de apoyo multidisciplinarios
- TORS (Cirugía transrobótica transoral) o TOUSS (TransOral endoscopic UltraSonic Surgery) . Las resecciones por medio del robot Da Vinci, o mediante el TOUSS, mejoran a nuestro entender la exposición de estos tumores, por la gran calidad de imagen, aunque dado su elevado costo, de estos sistemas tendrán que mejorar los resultados con los procedimientos habituales endoscópicos, ya ampliamente implantados en los servicios oncológicos de ORL.
Opción conservadora: Radioterapia radical. Tanto a nivel laríngeo como cervical.
T3-4 N0 supraglótico
Opción conservadora (primera opción en nuestro protocolo) : QT/RT concomitante - T4 N0 supraglótico, resecable, sin destrucción de cartílago, sin que exista invasión importante de la base de la lengua y/o afectación cutánea:
Opción quirúrgica: Laringuectomía total con hemitiroidectomía ipsilateral, y vaciamiento selectivo bilateral. La preservación de la laringe con quimiorradioterapia concurrente se debe considerar para los tumores T4, a menos que haya invasión tumoral a través del cartílago hacia los tejidos blandos del cuello, en cuyo caso la laringectomía total produce mejores resultados Cuando el estudio de las piezas quirúrgicas informa de no afectación ganglionar, afectación de un solo ganglio, o ausencia de rasgos desfavorables: RT adyuvante opcional. En presencia de rasgos desfavorables: QT/RT.
Valorar quimioterapia neoadyuvante en casos de complejidad quirúrgica o para facilitar el manejo operatorio, seguida de laringectomía total, ampliada o no, hemitiroidectomía ipsilateral y vaciamiento selectivo bilateral. Quimiorradioterapia postoperatoria.
En T3, en ausencia de evidencia clínica o radiológica de enfermedad ganglionar, se recomienda el tratamiento electivo - RT y / o disección selectiva del cuello al menos a nivel de los ganglios linfáticos II, III, IV bilateralmente. En T4, los niveles de ganglios linfáticos II-V bilateralmente deben tratarse, independientemente del estado ganglionar clínico previo al tratamiento
T4 N0 supraglótico, no resecable. QT/RT concomitante.
T1-2 N+ supraglótico.
Opción quirúrgica: Laringuectomía parcial horizontal supraglótica por vía endoscópica láser, TORS, o por vía externa clásica, con vaciamiento cervical bilateral. Si se ha optado por la vía endoscópica, se puede demorar el vaciamiento dos o tres semanas. RT adyuvante y ante rasgos desfavorables en las piezas, considerar RT/QT.
Opción mixta: Vaciamiento cervical bilateral seguido de radioterapia radical en laringe y cuello.
Opción conservadora. Quimio/Radioterapia concomitante.
T3-4 N+ supraglótico resecable,
Sin destrucción de cartílago y/o afectación leve de la base de la lengua.
Opción quirúrgica: La quimioterapia neoadyuvante está indicada en casos de complejidad quirúrgica o para facilitar el manejo operatorio. Se sigue con laringuectomía total ampliada o no, con doble vaciamiento cervical, seguida de RT adyuvante si no hay factores desfavorables en las piezas quirúrgicas, o RT/QT si los hay.
Opción conservadora: Quimio/Radioterapia concomitante.
T4 masivo N+ supraglótico resecable, con destrucción cartilaginosa
Invasión importante de la base de la lengua y/o afectación de la piel: Con o sin quimioterapia de inducción, laringectomía total, ampliada o no, con hemitiroidectomía ipsilateral y vaciamiento cervical bilateral. RT adyuvante si no hay factores desfavorables, y QT/RT concomitante si los hay.
T4 N+ supraglótico no resecable: QT/RT concomitante.
Láser C02. Exéresis lesión supraglótica
Laringectomía supraglótica por Da vinci
Laringectomia supraglotica abierta
* Quimio/RT postoperatoria (factores desfavorables) en los casos de uno o dos factores mayores adversos (afectación ganglionar extracapsular y márgenes quirúrgicos afectos) ó dos o más factores menores (afectación múltiple ganglionar sin afectación extracapsular, pT3 pT4, afectación ganglionar en niveles IV ó V, invasión perineural y embolismo vascular). o Radioterapia postoperatoria si existen menos de dos factores menores de riesgo (afectación múltiple ganglionar sin afectación extracapsular, pT3 pT4, afectación ganglionar en niveles IV ó V, invasión perineural y embolismo vascular).
- El papel de la quimioterapia de inducción antes de la quimiorradioterapia o la cirugía no está claro, pero puede ser apropiado para pacientes que presentan enfermedad ganglionar avanzada (por ejemplo, N2c / N3), particularmente si esto es rápidamente progresivo y / o sintomático.
En T1-2, los resultados de supervivencia parecen ser similares con la RT y la cirugía aunque, una vez más, no hay datos comparativos aleatorizados.
Mientras que los resultados funcionales a largo plazo (voz y deglución) parecen similares, la función de deglución temprana suele ser peor después de la cirugía: la rehabilitación por deglución puede prolongarse y en una pequeña proporción de pacientes, es posible que nunca se logre una función de deglución adecuada.
En consecuencia, la selección del paciente, basada en la carga del tumor y el estado funcional, es imprescindible.
Una vez más, se debe hacer todo lo posible para evitar combinar la cirugía con la RT porque los resultados funcionales pueden verse comprometidos por la terapia de modalidad combinada.
Todas las opciones de tratamiento parecen afectar el control locorregional y las tasas de supervivencia similares: para la enfermedad T1, las tasas de control local a cinco años después del tratamiento con RT, Láser C02, TORS o laringectomía supraglótica abierta varían del 77 al 100 por ciento.
Para los tumores T2, las tasas de control local a cinco años oscilan entre 80 y 97 por ciento para Láser o laringectomía supraglótica abierta y de 62 a 83 por ciento para RT primaria.
Los principios de preservación de órganos para cánceres supraglóticos T3 son los mismos que para cánceres glóticos. El tamaño del tumor, la función laríngea previa al tratamiento y el estado funcional deben dirigir el tratamiento de pacientes individuales. Las tasas de laringectomía de rescate después del tratamiento quirúrgico y no quirúrgico de los cánceres supraglóticos son más bajas que las de los cánceres glóticos. La función de las cuerdas vocales, generalmente está bien preservada después de laringectomía supraglótica endoscópica, o laringectomía supraglótica; sin embargo, la rehabilitación de la función de deglución después de la cirugía supraglótica puede prolongarse y, aunque la mayoría de los pacientes logran una función satisfactoria de deglución, esto no puede garantizarse.
Según el ensayo clínico PET-Neck de Mehanna, los pacientes T3, con enfermedad del cuello N2 o N3 que se someten a tratamiento con quimiorradioterapia como opción terapéutica, y experimentan una respuesta completa con una PET-TC posterior postratamiento negativa no requieren disección planeada del cuello. Por el contrario, los pacientes que tienen una respuesta parcial al tratamiento o que tienen una captación aumentada en una PET-TC después del tratamiento deben someterse a una disección del cuello.
Los pacientes con tumores T4 de gran volumen que no son aptos para la cirugía debido a una enfermedad inoperable (T4b) han recibido tratamiento de preservación de órganos de modalidad combinada con tasas significativas de control de la enfermedad (71% a los cuatro años) y supervivencia general (56% a los cuatro años) en estudios retrospectivos
Nos referiremos brevemente a las complicaciones de las modalidades terapéuticas utilizadas: la cirugía laríngea, el vaciamiento cervical, la radioterapia y la quimioterapia.
- Complicaciones secundarias a cirugía laríngea directa: Dolor regional que puede aparecer a largo plazo hasta en un tercio de los pacientes, Problemas de la voz, que mejora rápidamente en cirugías supraglóticas y que tendremos que rehabilitar en laringectomías totales. Deglución, la cirugía sobre la supraglotis altera la anatomía y la sensibilidad de este órgano, produciéndose frecuentemente aspiraciones y disfagia por alteración de la fase faríngea de la deglución.
- Por cirugía del vaciamiento cervical, ya resumidas en el consentimiento informado de la SEORL-PCF: hemorragia, infección de la herida quirúrgica con dehiscencia de suturas y hasta necrosis. Complicaciones cardiovasculares: shock hipovolémico, embolia gaseosa, trombosis venosa, embolia pulmonar y paro cardíaco. Daños isquémicos neurológicos: ceguera, HNS, vértigo, hemiplejia, muerte; problemas respiratorios (la traqueotomía que se realiza habitualmente, bien durante la cirugía asociada del tumor primario, bien de forma profiláctica antes de realizar el tratamiento RQT, solventaría estos problemas); lesiones nerviosas: hipogloso (lengua), espinal (hombro), frénico (diafragma), plexo braquial (problemas sensitivos y motores de la EESS), auricular mayor (adormecimiento pabellón auricular); ulcus péptico por estrés; lesión del conducto torácico (lado izquierdo: abombamiento y fistulización cervical de líquido lechoso); cicatriz antiestética.
- Propias de la radioterapia, que pueden ser efectos secundarios agudos o crónicos. En la orofaringe, la complicación aguda más frecuente es la mucositis.
La mucositis es más grave en los protocolos que combinan concomitantemente RT y QT, y suele mejorar al terminar la RT.
Otra complicación aguda frecuente es la alteración del gusto por destrucción de las papilas gustativas, que suele recuperarse a los 2 meses de finalizar el tratamiento.
La complicación crónica más frecuente es la xerostomía por la lesión salival de la RT, que se puede limitar con el uso de amifostina y glutamina intravenosa para proteger las mucosas y con técnicas de irradiación más selectivas del tipo radioterapia de intensidad modulada.
Otros son: la caries (revisión dental previa e higiene oral adecuada), el trismus (fibrosis muscular o articular), la osteorradionecrosis (más frecuente en cirugías previas de mandíbula y en pacientes con caries mal tratadas), astenia y anorexia (hasta 6 semanas después de finalizar la RT), cambios tróficos de la piel (peor en esquemas de RQT), caída del cabello (recuperación a los 3 meses).
Es importante descartar en estos pacientes la aparición de un hipotiroidismo subclínico mediante determinaciones hormonales (TSH y T4).
La mielitis posradioterápica es una complicación rara (medidas de protección) pero grave en el tratamiento de los tumores de la vía aerodigestiva superior, producida por devascularización de la médula espinal (incluso varios meses después de terminar la RT).
- Los efectos secundarios más frecuentes de la quimioterapia: neutropenia (factor estimulante de granulocitos), náuseas y vómitos, nefrotoxicidad, anemia, diarrea y sepsis.
- National Comprehensive Cancer Network: Clinical Practice Guidelines in Oncology (NCCN Guidelines®). Head and Neck cancers. Version 1.2018. NCCN.org.
- Functional outcomes of supraglottic squamous cell carcinoma treated by transoral laser microsurgery compared with horizontal supraglottic laryngectomy in patients younger and older than 65 years. Chiesa Estomba CM, Betances Reinoso FA, Lorenzo Lorenzo AI, Fariña Conde JL, Araujo Nores J, Santidrian Hidalgo C. Acta Otorhinolaryngol Ital. 2016 Dec;36(6):450-458. doi: 10.14639/0392-100X-864.
- Laryngeal cancer: United Kingdom National Multidisciplinary guidelines. Jones TM, De M, Foran B, Harrington K, Mortimore S. J Laryngol Otol. 2016 May;130(S2):S75-S82. PMID: 27841116
- Simo R1 , Bradley P, Chevalier D, Dikkers F, Eckel H, Matar N, Peretti G, Piazza C, Remacle M, Quer M. Eur Arch Otorhinolaryngol. 2014 Sep;271(9):2469-79.
- Epidemiology of laryngeal cancer: results of the Heidelberg case-control study. Maier H, Tisch M. Acta Otolaryngol Suppl. 1997;527:160-4.
- Epidemiology of laryngeal cancer. Cattaruzza MS, Maisonneuve P, Boyle P. Eur J Cancer B Oral Oncol. 1996 Sep;32B(5):293-305.
- Review. Detección simultánea del HPV-6b y 16 en el cáncer faringolaríngeo. Álvarez I, Sánchez P, Ramos S, Rodrigo JP, Llorente JL, Suárez C. Acta Otorrinolaringol Esp, 1996; 47:93-96.
- Laryngeal cáncer and gastroesophageal reflux disease: a case-control study. Vaezi MF, Qadeer MA, López R, Colabianchi N. Am J Med, 2006; 119:768-776.
- Study of laryngopharyngeal reflux using pH-metering in immediate post-op of laryngectomized patients. Marín Garrido C, Fernández Liesa R, Vallès Varela H, Naya Gálvez MJ. Acta Otorrinolaringol Esp. 2007 Aug-Sep;58(7):284-9. Spanish.
- Supraglottic and glottic carcinomas. Study of the incidence in the last 31 years.Tamarit Conejeros JM, Carrasco Llatas M, Estellés Ferriol E, Fernández Martínez S, Baviera Granell N, Dalmau Galofre J. Acta Otorrinolaringol Esp. 2007 Dec; 58(10):449-53.
- Metástasis a distancia en pacientes con carcinoma de laringe avanzado. Lahoz Zamarro et al. Acta Otorrinolaringol Esp 2001; 52: 307-311.
- Modalidades de preservación de órgano en carcinomas de laringe e hipofaringe. Miquel Quer y Xavier León. Acta Otorrinolaringol Esp 2007; 58(10): 476-82.
- Mortalidad en el cáncer de laringe en estadios avanzados. Lahoz Zamarro et al. Acta Otorrinolaringol Esp 2001; 52: 494-500.
- León X, Quer M, Orús C, Venegas MP, Montoro V. Distant metastases in head and neck cáncer patients who achieved loco-regional control. Head Neck, 2000: 22:680-686.
- León X, Quer M, Diez S, Orús C, López-Poussa A, Burgués J. Second neoplasm in patients with head and neck cáncer. Head Neck, 1999; 21:204-210.
- A surgeon looks at cervical lymph nodes. Johnson JT. Radiology. 1990 Jun;175(3):607-10. Review.
- Mehanna H, Wong WL, McConkey CC, Rahman J, Robinson M, Hartley A et al. PETCT surveillance versus neck dissection in advanced head and neck cancer. N Engl J Med 2016;374:1444–54
 Pasar al contenido principal
Pasar al contenido principal